先端ナノ・バイオ科学専攻 Major of Advanced Nanociences and Biosciences
Synthetic and mechanistic studies of highly functional metal complexes
 ナノサイズ機能性分子設計学 Nano-Size Functional Molecule Design Chemistry
ナノサイズ機能性分子設計学 Nano-Size Functional Molecule Design Chemistry會澤 宣一 Sen-ichi Aizawa
- TEL : 076-445-6980
- URL : http://www3.u-toyama.ac.jp/saizawa/group/
- Keywords : Transition metal complexes, Molecular orbital, Reaction Mechanism, Selective coordination, Catalytic activity, NMR shift reagent
研究の背景と目的 Background and Purpose of Study
生体内において、金属イオンは極めて高い機能を有し、重要な役割を果たしている。我々が、このような生体内金属活性部位(metallobiosite)に匹敵する機能を有する金属錯体を合成するためには、設計する金属錯体の電子状態(electronic state)、立体化学(stereochemistry)、反応機構等(reaction mechanism)の詳細についての理解が必要である。そこで我々は、目的とする機能を有する錯体を設計するために、熱力学的および速度論的検討に基づいた金属錯体試薬や材料の開発を進めている。現在は、金属錯体の配位選択性や酸化状態の精密な制御を試みている。
Metal ions play functionally quite important role in vivo. In order to design such a highly functional metal complex, we need to understand the electronic, steric, and mechanistic details of the complex. Accordingly, we are developing new functional metal complexes on the basis of thermodynamic and kinetic studies. Our present aim is to control the coordinative selectivity and oxidation state of the transition metal ions to apply the metal complexes to new medicines and materials.
本研究の領域横断性
金属錯体の反応機構や機能発現のメカニズムを解明することは、生体内金属活性部位の高度な機能を理解するためにも必須である。これにより、我々も生理活性部位に匹敵する、あるいはそれを超えた機能を有する金属錯体を設計できるようになり、有効な薬剤の開発へもつながる。この点に関しては、医薬理工の領域横断性が将来的に強まる分野である。さらに、生理活性の発現には、活性部位の特性だけでなく、金属錯体と生体内の外圏環境との相互作用が重要な場合が多く、領域横断性が必然的に要求される分野でもある。
研究内容
I. 金属錯体の安定度を決定する要因に対する新しい解釈
1) d電子反発の大きな寄与
これまで、遷移金属錯体の安定度はしばしば配位子場理論を用いて議論されてきたが、配位数の異なる金属錯体の安定度を比較する場合、配位子場分裂を生じないと仮定した球対称の金属イオンのd軌道のエネルギー準位の違いを考慮しなければならない。また、金属錯体の反応機構も、しばしば配位子場に関連付けて議論されてきたが、遷移状態と基底状態の配位数が異なる場合は議論できない。近年、純アミン溶媒中で、Co(II)イオンの四配位と六配位の幾何平衡が観測された(文献1,2)。そこで、それぞれの幾何配置の配位子場安定化エネルギー(LESE)を吸収スペクトルから計算し、両幾何配置間のエンタルピー差(ΔH0)を平衡定数の温度依存性より実験的に求めて、両配位数間の球対称イオンのエネルギー差(ΔΕspher)を計算した(Fig. 1)。
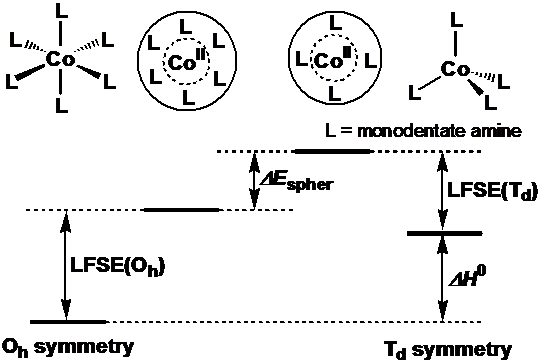 Fig.1. Octahedral–tetrahedral equilibrium.
Fig.1. Octahedral–tetrahedral equilibrium.
この結果、錯体の安定度を決定する要因として、LSFEの違いよりもΔΕspherの違いが大きく寄与していることが明らかになった。さらに、ΔΕspherの違いは、d電子間反発パラメーターの大きさと良い相関があり、錯体間の安定度を比較する場合は、LFSEだけでなくd電子反発のパラメーターの比較が必須であるとが示された(文献2)。
2) キレート効果の本質
これまでキレート化合物の安定性(キレート効果)は、錯形成に伴う分子数の減少が単座配位子の場合より少ないというエントロピー効果によって説明されてきた。しかしながら、特にσ結合性の強い錯体のキレート効果は非常に大きく、五員環、六員環といったキレート環の大きさにも大きく依存する。これらの事実は、エントロピー効果だけでは説明できない。そこで、解離的反応機構を有する遷移金属錯体について、エチレンジアミン(en、五員環)、1,3-プロパンジアミン(tn、六員環)、n-プロピルアミン(単座)の溶媒交換速度をNMR法で測定した。その結果、五員環、六員環、単座の順に交換反応の活性化エンタルピー(ΔH‡)が顕著に減少することがわかった。この研究より、イオン結合性、π結合性、σ結合性といった結合性の違いや、五員環、六員環といった、キレート環の大きさの違いによる、キレート効果の大きさの違いが説明できるようになった(文献1,3,4)。
II. 基礎研究に立脚した機能性錯体の開発
1) 高い配位選択性を有する金属錯体
Pd(II)およびPt(II)は通常四配位平面型錯体を形成するが、Fig. 2のような三脚状四座ホスフィン配位子(pp3)を用いると、五配位三角両錐型錯体を形成しやすくなる(文献5)。4配位平面型錯体では、酸素、窒素、硫黄、リンなどの供与原子を配位できるが、これまでの基礎研究から、五配位三角両錐型錯体では電子反発が大きいために、酸素や窒素原子よりも硫黄やリン原子に対して選択性が高まると考えられる。そこでpp3を有する五配位三角両錐型錯体[Pd(pp3)(CNCH3)]2+とL-システィネート(L-cys)との反応を行ったところ、チオラト硫黄原子でL-cysが単座配位した五配位三角両錐型錯体が生成した。また、複数の含硫および非含硫アミノ酸の中から、L-cysのみを選択的に配位することにより分離でき、還元型グルタチオンのチオラト硫黄原子のみを単座配位して定量することができた。直鎖状三座ホスフィン配位子(p3)を有する四配位平面型Pd(II)錯体においては、酸素、窒素ドナーで配位できるため、上述のようなチオラト硫黄に対する高い選択性は生じなかった。
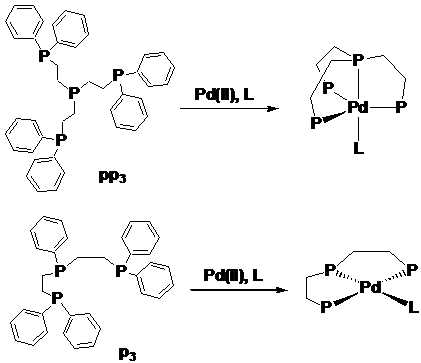 Fig.2. Pd(II) complexes with pp3 and p3.
Fig.2. Pd(II) complexes with pp3 and p3.
2) 重金属イオンを同定、定量できるトリス(チオラト)錯体
隣り合う3つのチオラト硫黄原子を持つ光学活性錯体Δ-fac(S)-[M(L-cys-N,S or aet)3]3- or 0(M = Rh(III) or Co(III))(1)は、fac位のチオラト硫黄が種々の重金属イオンに架橋することによって、チオラト硫黄の孤立電子対の反発が避けられるため、安定な硫黄架橋多核錯体(2)を形成する(Fig. 3)。この多核錯体は不斉硫黄が架橋した金属イオンに特徴的な強度の強いCDスペクトルを示すため、重金属イオンの同定、定量が感度よく行える。さらに、錯体ユニットをポリアリルアミンにアミド架橋することにより、重金属、貴金属イオンのみを分離・濃縮・同定できる錯体ポリマー(3)を合成した(Fig. 3)(文献6)。
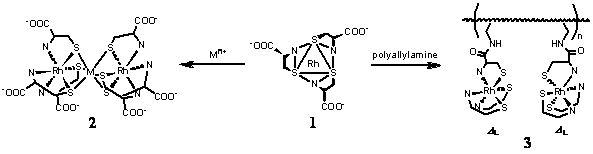 Fig. 3. Structures of Δ-fac(S)-[M(L-cys-N,S)3]3- (1), S-bridged complex (2),
and peptide bridged polymer (3).
Fig. 3. Structures of Δ-fac(S)-[M(L-cys-N,S)3]3- (1), S-bridged complex (2),
and peptide bridged polymer (3).
3) 空気中でも安定で再生・再利用可能なPd(0)錯体触媒の開発
これまで、有用な有機合成反応触媒としてホスフィンを配位子とするPd(0)錯体が広く用いられてきたが、ホスフィンは空気中で酸化されやすく、これに伴いPd(0)錯体はPd黒に分解するため、触媒の再生・再利用は極めて困難であった。そこで、ホスフィンを硫黄化することにより酸化を防ぎ、ホスフィンスルフィドのπ受容性によりPd(0)を安定化することにより、空気中でも安定でしかも繰り返し利用できるPd(0)錯体触媒を合成した。また、ホスフィンカルコゲニドのカルコゲン原子交換反応に対するPd(0)の新規触媒活性が見出されたため、これを用いて、酸化されたホスフィンから容易にフォスフィンスルフィドPd(0)錯体触媒を再生することに成功した。さらに、ホスフィンスルフィドPd(0)錯体部分を担持させたポリマーを合成して、リサイクルが容易な実用に耐えうる固体触媒を開発した(Fig. 4)(文献7)。
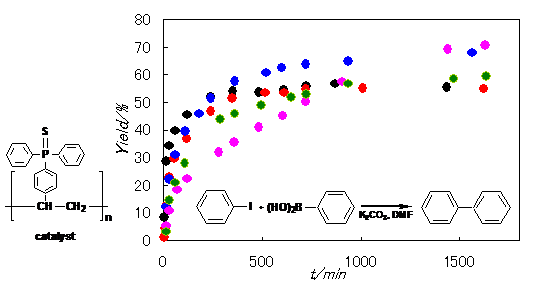 Fig.4. Change in the yield of biphenyl with time in Suzuki coupling reaction catalyzed by the Pd(II) polymer (●, freshly prepared; ●, recycled once; ●, recycled twice; ●, recycled three times; ●, recycled four times) in the air.
Fig.4. Change in the yield of biphenyl with time in Suzuki coupling reaction catalyzed by the Pd(II) polymer (●, freshly prepared; ●, recycled once; ●, recycled twice; ●, recycled three times; ●, recycled four times) in the air.
4) 食品の真正証明に応用できる実用的なNMRキラルシフト試薬の開発
食品中に含まれる天然の有機酸やアミノ酸はL体であるが、人工添加物中ではほとんどの場合DLラセミ混合物である。そこで、光学異性体を個別に同定するための、クロマトグラフ法やキャピラリー電気泳動法が開発されてきた。しかしながらこれらの方法は混合物である実試料分析においてはシグナルの重なりが分析の妨げになる。また、シグナルの流動速度は実験条件によって大きく変化するため、標準試料によるシグナルの帰属が必要となる。一方、NMR法は分子中のそれぞれの原子についてシグナルが観測されるため、全てのシグナルが重なることはなく、混合物の分析には適する。また、既知化合物なら標準試料なしで化学シフト値から化合物の同定ができる。そこで、キラルシフト試薬を用いた光学活性体のNMR分析が考案されてきた。しかしながら、現在用いられているキラルシフト試薬は高価な合成多座配位子を有するランタノイド錯体が主流である。さらに、現在通常使用されている超伝導NMR装置は大変高価で、液体ヘリウムや液体窒素を冷媒として使用しているため、維持費も高く、装置を移動して現場で分析することは不可能である。また、磁場が大きいほど、常磁性金属イオンの影響でシグナルの広幅化が顕著になり、キラル分離分析の妨げになる。そこで本研究では、NMR法の利点を食品の真正システムに利用するために、1.安価な光学活性アミノ酸や有機酸を用いて、分子中に不斉点を複数持つキラル識別能が高い配位子を開発し、磁気異方性が大きいランタノイドイオンを用いて微量の試薬で分析を可能とした(Fig. 5)。今後、汎用金属イオンを用いたり、永久磁石を備えた低磁場NMRを取り入れることを目指している(文献8)。
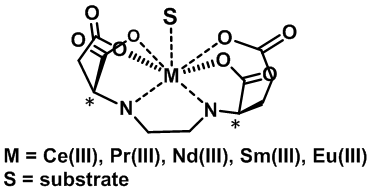 Fig. 5. Ethylene-bridged-L- aspartate complexes
Fig. 5. Ethylene-bridged-L- aspartate complexes
参考文献
- S. Aizawa, S. Iida, K. Matsuda, and S. Funahashi, Inorg. Chem., 35, 1338-1342 (1996).
- S. Aizawa and S. Funahashi, Inorg. Chem., 41, 4555-4559 (2002).
- S. Aizawa, K. Matsuda, T. Tajima, M. Maeda, T. Sugata, and S. Funahashi, Inorg. Chem., 34, 2042-2047 (1995).
- S. Aizawa, S. Iida, K. Matsuda, and S. Funahashi, Bull. Chem. Soc. Jpn., 70, 1593-1597 (1997).
- S. Aizawa, T. Iida, S. Funahashi, Inorg. Chem., 35, 5163-5167 (1996).
- S. Aizawa, S. Tsubosaka, Chirality, 28, 85-91 (2016).
- S. Aizawa, A. Majumder, Y. Yokoyama, M. Tamai, D. Maeda, and A. Kitamura, Organomet. 28, 6067-6072 (2009).
- S. Aizawa, T. Kidani, S. Takada, Y. Ofusa, Chirality, 27, 353-357 (2015); S. Aizawa, M. Okano, T. Kidani,, Chirality, 29, 273-281 (2017).

